Wirkungsvollere Medikamente mit Nanopartikeln
Projekt „Nanokapseln zum kontrollierten Medikamenteneinschluss“
Projektlaufzeit
Oktober 2012 bis April 2017
Zielsetzung
Bei der gezielten Verabreichung von Medikamenten haben Nanopartikel großes Potenzial als maßgeschneiderte Medikamententräger, sogenannte „drug carrier“. Sie ermöglichen, dass Wirkstoffe in kleinsten Portionen transportiert und gezielt freigesetzt werden können. Ein essentieller Punkt hierbei ist der kontrollierte und präzise Einschluss von diskreten Medikamentenvolumina und Konzentrationen in Nanokapseln. Nur eine gute Kontrolle dieses Einkapselungsprozesses ermöglicht die spätere genau dosierte Abgabe des Wirkstoffs, sei es in Form eines Aerosols, intravenös oder als Implantat.
Bisherige Verfahren erlauben den Medikamenteneinschluss bis zu einigen Mikrometern. Für den Einsatz als „drug carrier“ in der medizinischen Praxis sind aber meist Nanokapseln deutlich unter 1 Mikrometer im Nanometerbereich erforderlich. Um dieses Ziel zu erreichen, plante die Arbeitsgruppe von Prof. Dr. Franke neue technische Verfahren zu entwickeln. Dadurch wird ein über die medizinische Applikation hinausgehendes Anwendungspotential erschlossen, das beispielsweise auch hochinteressant für die Biotechnologie ist. Biologische Makromoleküle, wie DNA oder Proteine, lassen sich hierdurch gezielt einkapseln und mit anderen Kapseln, die biologische Zellen enthalten, kombinieren, um Reaktionen mit diesen Zellen zu studieren.
Die Forschungsarbeiten wurden zusammen mit der „School of Engineering and Applied Sciences“ der Harvard Universität durchgeführt. Die enge Zusammenarbeit mit dieser weltweit führenden Gruppe ermöglichte es mit der schnellen Entwicklung auf diesem Gebiet Anschluss zu halten. Eine weitere Kooperation bestand zur Gruppe von Prof. Dr. Gabor am Lehrstuhl für Pharmazeutische Technologie und Biopharmazeutik der Universität Wien. Diese Gruppe brachte ihre Expertise zur Funktionalisierung und Charakterisierung von Mikro- und Nanopartikeln in der Medizin ein.
Ergebnisse
Im Forschungsvorhaben „Nanokapseln zum kontrollierten Medikamenteinschluss“ der Universität Augsburg wurde ein System entwickelt, welches das Sortieren von Mikropartikeln in einer Flüssigkeit ermöglicht und als Grundlage für Anwendungen in Biotechnologie, analytischer Chemie und Medizin dienen kann.
Dazu wurde ein mehrlagiger Mikrokanal aus dem Kunststoff Polydimethylsiloxan (PDMS) entworfen, dessen obere Schicht die Kanalstruktur enthält. In der wenige Mikrometer dünnen Unterschicht befindet sich ein sogenannter interdigitaler Transducer (IDT), der es erlaubt, eine akustische Oberflächenwelle in den Mikrokanal einzukoppeln.
Diese lokale Einkopplung einer angeregten akustischen Oberflächenwelle erlaubt dann die kontrollierte Ablenkung und den Transport von Mikropartikeln im Kanal (1). Das entwickelte System ist auch in der Lage, Partikel experimentell „zu waschen“, d. h. sie unbeschadet in ein anderes Lösungsmittel zu überführen.
Basierend auf diesen Arbeiten wurde ein Bandpassfilter entworfen und experimentell realisiert. Der Filter beruht ebenfalls auf akustischen Oberflächenwellen und ermöglicht das Filtern und Sortieren von Mikropartikeln im Mikrokanal (Abbildung 1). Die Forschungsergebnisse wurden in der Zeitschrift „Microfluidics and Nanofluidics“ veröffentlich (2).
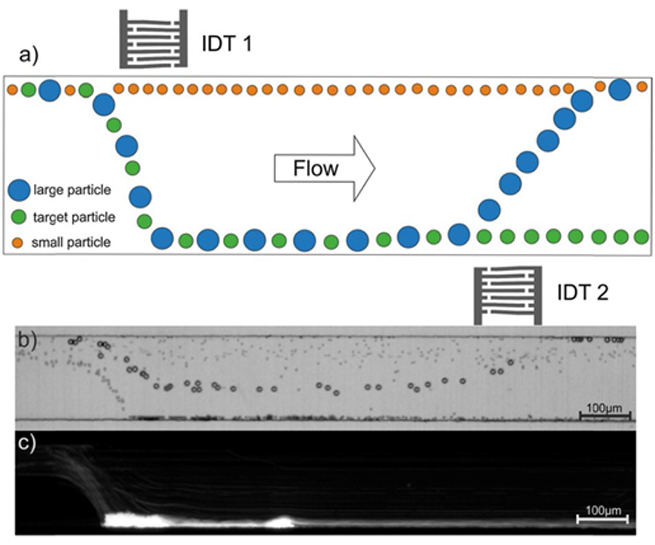
Abbildung 1: a) Schematischer Aufbau des Bandpassfilters. Die Flüssigkeit transportiert Partikel verschiedener Größen von links nach rechts. Ein zusätzlicher Einlass fokussiert alle Partikel oben. Die größeren Partikel (blau und grün) werden von der ersten über einen interdigitalen Transducer (IDT) erzeugten Oberflächenwelle nach unten abgelenkt. Die kleinsten Partikel (rot) werden aufgrund ihrer geringen Größe nicht beeinträchtigt. Bei der zweiten generierten Oberflächenwelle (größere Wellenlänge) werden analog nur die größten Partikel (blau) abgelenkt. Insgesamt werden so nur die Partikel der gewünschten Größe (grün) nach unten abgelenkt, während die restlichen Partikel am oberen Rand des Kanals verbleiben. b) Mikroskopbild einiger überlagerter Bilder, um die Bahnen der Partikel verschiedener Größen (3 µm, 4,5 µm und 10 µm) zu veranschaulichen. c) Fluoreszenzaufnahme der gefilterten 4,5 µm großen Partikel. Diese werden bereits von der ersten Oberflächenwelle nach unten abgelenkt. Die zweite Oberflächenwelle lenkt diese Partikelgröße nicht ab.
Da zur gezielten Anwendung der Oberflächenwelle genauere Kenntnisse über interdigitale Transducer und Oberflächenwellen, wie z. B. Schallpfadbreite der Welle, benötigt werden, wurde eine Methode zum einfachen Sichtbarmachen und zur Charakterisierung der Oberflächenwelle in Kooperation mit der Universität Glasgow über Laser-Vibrometermessungen erforscht (3).
Die präzise Bestimmung und Kontrolle des Schallpfades hat es nun möglich gemacht, ein weiteres sehr wichtiges Anwendungsfeld zu erschliessen, nämlich die Qualitätskontrolle von sogenannten „Lab on a Chip Systemen“ in Echtzeit. In solchen miniaturisierten Systemen werden häufig Tropfen mit einem Durchmesser von 1/100 Millimeter (10 µm) als kleinste Reaktionsgefässe verwendet und seriell mit Raten von bis zu 1000 Tropfen pro Sekunde prozessiert. Mit der gezielten und genau lokalisierten Anwendung einer akustischen Oberflächenwelle war es nun zum ersten Mal möglich, einzelne Tropfen im „laufenden Screening Betrieb“ zu entnehmen und für Messungen zu immobilisieren (Abbildung 2) ohne den Ablauf des Screenings oder die Reihenfolge der prozessierten Tropfen zu beeinträchtigen (4, 5).

Abbildung 2: Dreidimensionales Design einer Tropfenfalle zur Immobilisierung und Vermessungen einzelner Tropfen, die aus einem kontiniuierlich fliessenden Tropfenversuch selektiv entnommen werden. A: der blaue Tropfen ist in der Falle lokalisiert. B: Mittles eins akustischen Pulses (SAW) wird er wieder dem System zugeführt C: ein weiterer Tropfen (rot) wird in der Falle eingefangen D: der rote Tropfen ist für Messungen immobilisiert und kann später bei Bedarf wieder entlassen werden.
Die erst seit einigen Jahren entwickelte Emulsionstropfen-Fluidik hat in vielen medizinischen und gesundheitsrelevanten Bereichen riesiges Potential und ist erst am Anfang ihrer Entwicklung. So kann beispielsweise in Tropfen die Resistenz von Bakterien auf verschiedene Antibiotika getestet werden und so bei höchsten Durchsatzraten ein Massentest (high throughput screening, HTS) mit noch nie da gewesenen Probenzahlen durchgeführt werden.
Antibiotika resistente Keime lassen sich so identifizieren und im Anschluss gezielt aussortieren und analysieren – ein wichtiges Problem bei der zunehmenden Resistenz von Krankenhauskeimen. Die extrem hohen Prozessierungsgeschwindigkeiten in solchen HTS-Sytemen machen eine Qualitätskontrolle der Tropfenprozessierung ohne den Ablauf des Screens zu behindern schwierig.
Detaillierte Informationen zu den Ergebnissen finden Sie hier:
- (1)
- Localization and shaping of surface acoustic waves using PDMS posts: application for particle filtering and washing. Richard W. Rambach, Viktor Skowronek and Thomas Franke. RSC Advances 4(2014), 60534-60542.
- (2)
- Surface acoustic wave controlled integrated band-pass filter. Viktor Skowronek, Richard W. Rambach and Thomas Franke. Microfluid Nanofluid 19 (2015), 335–341..
- (3)
- Visualization of Surface Acoustic Waves in thin Liquid Films. Richard W. Rambach et al. Scientific Reports 6 (2016) 21980-21989.
- (4)
- Single Droplets Trapping and Fast Acoustic Release in a Multi-height Device with Steady-state flow. R. W. Rambach, Kevin Linder, Michael Heymann and T. Franke, submitted
- (5)
- Selectively trapping and releasing of picoliter droplets in a 3D microfluidic PDMS multi trap system using bubbles. Richard W. Rambach, Preetika Biswas, Ashutosh Yadav, Piotr Garstecki and Thomas Franke, ready for submission
Weitere Informationen
Universität Augsburg
Lehrstuhl für Experimentalphysik I
AG Mikrofluidik/Biophysik
Prof. Dr. T. Franke
Universitätsstr. 1, 86159 Augsburg
Tel.: 0821-598-3312, Fax: 0821-598-3225


